核酸感受是机体免疫系统识别病原的重要方式之一。近日,大连医科大学肿瘤干细胞研究院杨庆凯、宋成丽等在《Cell》期刊上发表了题为《SARM1 senses dsDNA to promote NAD+degradation and cell death》的论文,指出SARM1是DNA的免疫感受器,其被DNA激活后,可降解NAD诱导细胞死亡。该项工作揭示了机体免疫识别的新机制,为改善肿瘤等疾病的综合防治效果提供了新思路和新靶点。

识别异我(non-self或abnormal-self)是机体免疫功能的基础。为识别众多的异我致病因子,生物进化出一种重要的免疫识别策略——核酸免疫感受,即通过识别异常核酸,激活免疫反应,实现对病毒和肿瘤等异我致病因子的清除。目前,基于核酸感受的干预手段已被广泛应用于临床,如临床广泛使用的放化疗等抗肿瘤治疗手段,可通过修饰损伤DNA,产生异常DNA,激活相关反应,进而清除肿瘤。然而,DNA感知机制十分复杂。现阶段,对人类细胞DNA感知的研究焦点,主要集中于环GMP-AMP合成酶(cGAS)等通过干扰素激活天然免疫感受器等过程,对其他机制则探索较少,存在一定的认知空白。
值得注意的是,后天免疫在进化上出现较晚,绝大多数生物不具后天免疫系统,却能有效清除病毒等异我。此外,脑和眼等体现出后天免疫豁免特性,异常DNA在肝和神经等细胞中难以诱导干扰素产生,神经等细胞基本不表达MHC(MHC与TCR的互作介导T细胞后天免疫),暗示后天免疫在某些细胞的异我清除中作用有限。有趣的是,上述细胞并未表现出对DNA病毒等异我的敏感性,说明某些DNA感受机制可能在其中起到关键作用。但目前对相关机制仍知之甚少,阻碍了相关临床干预手段的开发与应用。例如,一般认为旺盛分裂的细胞对化疗更敏感,但神经等不分裂细胞对化疗也较敏感,大部分肿瘤患者在化疗期均会遭受神经损伤,在相当数量的患者中甚至出现永久损伤,妨碍了临床治疗的开展与提升。
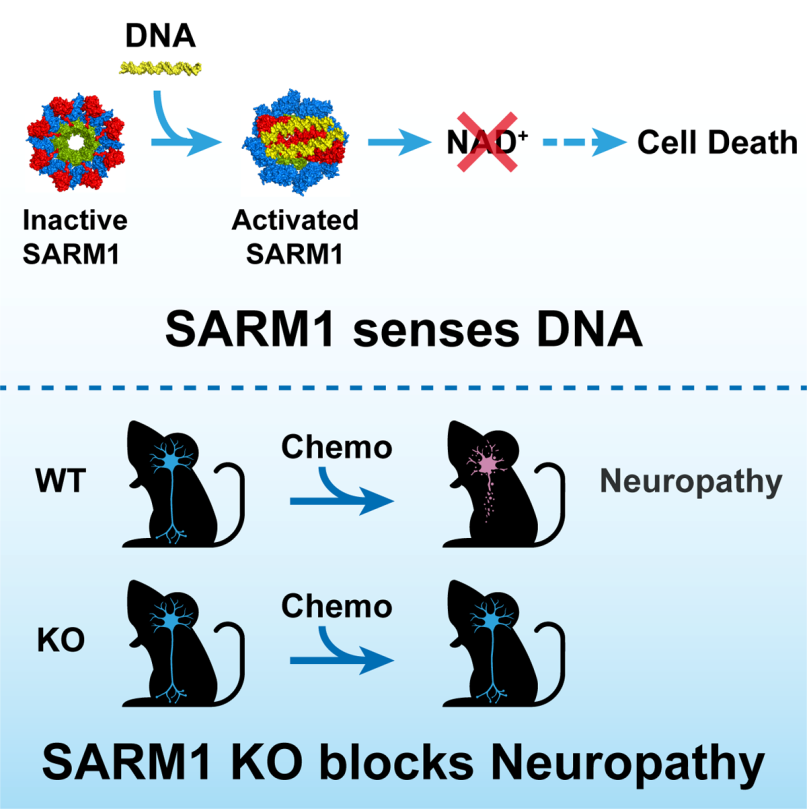
近日,我校肿瘤干细胞研究院杨庆凯、宋成丽团队发现:SARM1(Sterile alpha and TIR motif containing 1)是DNA感受器,其被DNA激活后,可导致NAD降解引起细胞死亡;SARM1感受病毒DNA通过细胞死亡抵抗病毒感染;化疗通过产生异常DNA,激活SARM1引起神经细胞死亡,而敲除SARM1能废除化疗诱导的神经损伤,相关工作揭示了DNA免疫感受的新机制。
研究人员通过筛选发现DNA能通过激活SARM1降解NAD。其中,DNA是以DNA序列非依赖的方式激活SARM1的,这使得该过程中DNA可以来源于众多生理病理过程,包括但不限于:感染、衰老和放化疗等。因故,SARM1可参与多种生理病理过程,可能是众多疾病的潜在治疗靶点。进一步机制研究表明,SARM1能通过TIR(Toll/interleukin-1 receptor)结构域与DNA结合。TIR结构域可降解NAD,是催化结构域,在进化上高度保守,故上述结果还提示TIR结构域蛋白家族可能是一个潜在的跨多物种的DNA感受器家族。
免疫系统既要有效识别异常DNA,又要高度耐受正常DNA;DNA激活SARM1不依赖其序列的,提示SARM1需其它机制辅助DNA识别。后续研究结果表明,SARM1与DNA复合体含有两个dsDNA分子,部分蛋白可通过预缩短DNA间距,促进DNA激活SARM1。作为典型的异常DNA来源,病毒无论如何突变,病毒始终面临个巨大挑战,其必须将相对较长的DNA凝聚到很小的病毒中,所以小间距是病毒DNA的普遍特征。故SARM1可通过小间距辅助识别异常DNA,小间距可能是DNA感受器识别异常DNA的通用机制。此外,SARM1可感受病毒DNA引起细胞死亡,进而抵抗病毒感染。与之相类似,化疗可以通过产生异常DNA,激活SARM1引起细胞特别是神经细胞死亡,而敲除SARM1则能废除化疗诱导的神经损伤,上述结果凸显了SARM1的潜在临床价值。
该篇论文是大连医科大学作为第一完成单位在《Cell》上发表的第二篇文章,也是我校连续第二年以第一完成单位在《Cell》上发表学术论文,由肿瘤干细胞研究院杨庆凯教授与宋成丽教授担任共同通讯作者,王丽娜与刘巧玲为共同第一作者,研究过程中得到了我校基础医学院李韶教授和附属第二医院马骁驰教授等合作者以及各职能部门的大力支持。此项工作在国际顶级期刊的发表,是我校科学研究水平和实力的集中体现,不仅开辟了新研究领域的新方向,更展现出了强大的临床转化潜力,标志着我校在相关研究领域取得了里程碑式的进步,实现了从源头创新到国际学术影响力的重大跨越。
近年来,大连医科大学坚持以科技创新为引领,持续优化科研生态,强化交叉融合与有组织科研,在高端成果产出方面不断取得突破。此次在《Cell》再次发表重大成果,充分证明了我校科研水平的持续提升与核心竞争力的显著增强。站在新的起点,我们期待在学校的持续赋能与多方支持下,催生更多引领性原创突破,涌现更多通向临床应用的新路径,为推动医学进步、服务人民健康贡献更多力量!
论文链接:https://doi.org/10.1016/j.cell.2025.09.026.
团队负责人介绍:

杨庆凯,二级教授,大连医科大学肿瘤干细胞研究院副院长,国家自然科学基金杰出青年科学基金项目(现青年科学基金项目A类)和优秀青年科学基金项目(现青年科学基金项目B类)获得者。2001年获得南开大学学士学位,2006年获得中科院遗传与发育生物学研究所博士学位,其后在美国Scripps研究所(TSRI)从事科研工作,2013年全职任大连医科大学肿瘤干细胞研究院教授。近年来,主要研究核酸先天免疫感受与肿瘤,揭示了系列基于核酸物理特性的免疫识别机制,以通讯作者在Cell、Immunity等期刊上发表研究论文多篇。